
第97期
出刊日:2022-01-12
返回上一層換肝後,肝癌為何還復發?
就肝癌治療而言,肝臟移植已被證實是有效的治療方法之一,且需符合換肝條件後才能進行,尤其肝腫瘤不能有血管侵犯及遠端轉移。但為何有少數病人換肝後仍復發呢?
諮詢/吳耀銘(臺大醫院癌醫分院副院長、臺大醫院外科部主治醫師、臺大醫學院外科教授)
撰稿/楊雅馨
一位50幾歲的男性是B肝帶原者,因檢查出肝發炎指數及甲型胎兒蛋白數值異常升高,經醫師安排檢詳細檢查,發現他肝臟有腫瘤,於是開刀切除,不料2年後又復發;由於家人願意捐肝,幾經考量,病人決定接受肝臟移植手術。然而,半年後的定期回診追蹤,發現肺部有一顆腫瘤是肝癌轉移而來!原以為換肝後就可以擺脫癌症,只可惜事與願違。醫師安排他接受胸腔鏡手術切除腫瘤,後續仍須定期追蹤治療。
在談換肝後肝癌為什麼還是會復發之前,首先要清楚針對肝癌病人的換肝準則。什麼樣的肝癌病人適合以肝臟移植來治療呢?臨床上關於肝臟移植的準則還真不少,如米蘭準則(Milan Criteria)、舊金山大學準則(UCSF criteria)甚至京都大學準則(Kyoto criteria)等等。
換肝需符合準則
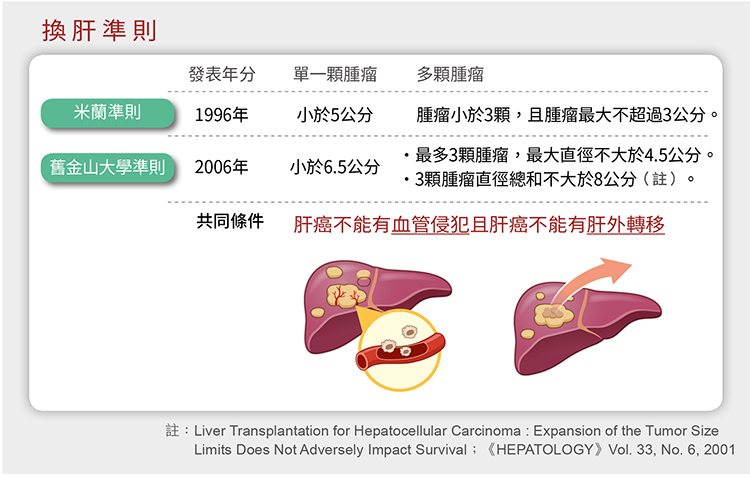
根據2017年《自然綜述:腸胃病學和肝臟病學》(Nature Reviews Gastroenterology & Hepatology)期刊的一篇研究顯示,採用米蘭準則的病人,其無復發存活率(Disease-free survival,DFS)4年有92%,移植後存活率(post transplantation survival)4年為85%;舊金山大學準則的病人其無復發存活率5年有90.9%,移植後存活率5年為80.9%;京都大學準則為無復發存活率5年有30%,移植後存活率5年有65%,也就是採用米蘭及舊金山準則的病人,存活數據表現較佳,因此,現在多以這兩者做為肝癌的換肝標準。
然而,米蘭準則比起舊金山大學準則更加嚴謹,以致於能符合標準做肝臟移植的肝癌病人並不多,但採用這兩者的患者存活率並無太大的顯著差異,因此,臨床上多以「舊金山大學準則」為原則。
兩前提需符合才能換肝
不過,不論採用哪個準則,有兩個重要的前提:一、肝癌沒有侵犯到血管;二、肝癌沒有轉移到肝外。符合這兩項條件的肝癌病人才適合做肝臟移植手術,其理由是換肝後必須長期服用抗排斥藥物治療,會削弱病人的免疫能力,若肝癌已侵犯血管或轉移肝外,換肝後將使體內殘餘癌細胞長的更快。
此外,除了腫瘤顆數、大小、血管侵犯、遠端轉移,還會將肝癌病理分期、血清的甲型胎兒蛋白(AFP)濃度列為移植評估參考指標,但想知道腫瘤的病理分期得有組織切片,不是每個病人都願意做肝穿刺檢查取得切片,所以臨床上常見的作法還是以甲型胎兒蛋白濃度作為主要偵測工具。
一般而言,病人術前的甲型胎兒蛋白濃度若在400∼500ng/ml以下(正常值應小於20ng/ml),術後復發的機率較低;若高於1000 ng/ml,術後復發的機率可能相對提高。
換肝後復發 多因有殘存癌細胞
即使肝癌移植標準符合最嚴謹的米蘭準則,仍然無法完全避免移植後肝癌復發,畢竟以現在的醫療科技,即使做了許多精密的檢查,也無法百分百確認體內沒有任何的癌細胞存在,而這些殘存的癌細胞也是肝臟移植後肝癌復發的主要原因。
一般而言,肝癌復發時間以移植後的第1∼2年發生率最高,2年後復發的機率就會逐漸趨緩,雖然,臨床上也是有5年後腫瘤才復發的案例,但並不常見。一旦肝癌復發,平均存活期約8.7個月,主要原因就是移植後病人必須使用抗排斥藥物造成免疫抑制,讓腫瘤的生長速度更快。
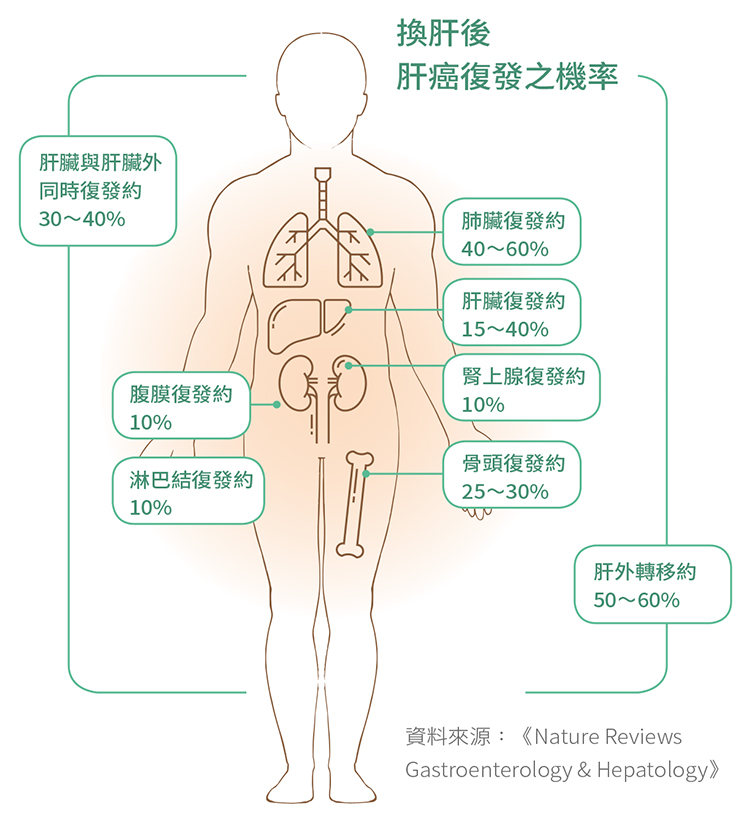
肝臟移植後肝癌復發,「肝外轉移」的比例遠高於「肝內轉移」,而「肝外轉移」最常見的侵犯器官是肺臟,其次為骨頭,腹腔、淋巴結、腎上腺等。
肝癌復發仍可採取相關治療
肝臟移植後的肝癌轉移,治療原則和一般的肝癌治療相同,都要依腫瘤大小、數目、位置、型態,以及病人的肝功能、身體狀況等作為評估。若僅有「肝內轉移」可先考慮做手術或電燒、栓塞等局部治療;若已發生「肝外轉移」則以手術治療、藥物治療為主,如單顆腫瘤轉移到肺臟,可以利用胸腔鏡將腫瘤切除,若全身轉移,目前的標準治療方式為標靶治療,免疫治療暫不列為選項之一,其理由是器官移植後必須吃抗排斥藥物將免疫力壓低,而免疫治療是要喚醒自體免疫細胞來殺死細胞,這兩者間就學理而言是互相衝突、矛盾。
至於,復發後能否二度換肝?臨床上並不建議,主要是體內已經有明顯的癌細胞存在,對病人的預後幫助不大,且二度換肝後病人的生活品質都不盡理想。
肝癌復發越能早期發現,治療效果越佳,因此移植後,定期回診更顯得重要,每次回診除了抽血檢測肝膽功能、甲型胎兒蛋白、抗排斥藥物的血中濃度,還包括腹部超音波或電腦斷層、磁振造影等影像學檢查。
抗排斥藥物與癌症復發的關聯
肝癌病人在肝臟移植後須終生服用免疫抑制劑以預防排斥反應,藥品的選擇需考量病人原發肝病(如B型肝炎、C型肝炎)、肝發炎指數、有哪些共病、是否有癌症復發或感染的危險因子等等,再依據藥品特性及藥品副作用等,選擇適當的免疫抑制劑,給予個別化與最佳化的治療劑量。
目前用於器官移植之免疫抑制劑有很多種,通常都會合併使用多種,以達到恢復正常的肝功能、抗排斥的目的,並降低各藥物副作用的發生率。如mTOR(mammalian target of rapamycin)抑制劑合併環孢靈素(Cyclosporine)、普樂可復(Prograf , FK506)等。
雖然有研究資料指出,使用mTOR抑制劑還可以抑制癌細胞復發,但還不是定論,仍需更多的研究及驗證。
術前評估是重要關鍵
未符合換肝標準仍有其他治療選項
即使是早期肝癌,亦有肝臟以外器官轉移之可能或血液中有肝癌細胞存在,乃是眾所皆知的事實,而這也是肝臟移植後肝癌復發的最主要原因,也因此,病人術前評估就顯得更為重要。
不過近年醫界對於是否一定要符合腫瘤大小與數目的標準才能做移植,有不同看法,有人認為非絕對禁忌,但就實際臨床觀察發現,若超過「舊金山大學準則」仍堅持換肝,對病人的存活率幫助很有限。事實上,目前晚期肝癌的治療已有進步,除了肝臟移植還有其他治療選項,如標靶治療、免疫治療,並不是只有肝臟移植一條路。
倘若符合「舊金山大學準則」且經醫師評估適合換肝,也不能猶豫太久,以不超過2∼3個月為原則,畢竟移植的時間點攸關腫瘤的生長速度。移植之後要配合醫師的指示密集的追蹤,尤其是在復發最常見的術後半年到2年間。
疑 惑 解 除 補 給 站
Q:肝癌患者早點做肝臟移植會比較好嗎?
A:在歐美國家,肝臟移植會列為肝癌的第一線治療,且以屍肝移植為主,活體肝臟捐贈較少;台灣目前仍建議優先考慮手術治療、電燒治療等,必要時才考慮肝臟移植,主因是屍肝捐贈少,8成患者得靠親屬捐肝。
A:在歐美國家,肝臟移植會列為肝癌的第一線治療,且以屍肝移植為主,活體肝臟捐贈較少;台灣目前仍建議優先考慮手術治療、電燒治療等,必要時才考慮肝臟移植,主因是屍肝捐贈少,8成患者得靠親屬捐肝。
雖然若能以肝臟移植作為肝癌治療第一選項,有較高的存活率,不過卻也得面臨日後長期使用抗排斥藥物所帶來的副作用,各有優缺點,很難說哪種一定比較好,且活體肝臟移植也需把捐贈者手術風險列入考量。
Q:肝癌病人接受親屬之間的活體肝臟捐贈,其肝癌復發的機率會高於屍肝移植嗎?
A:的確有這樣的說法,但目前仍無定論。主要原因是假如換肝病人體內已有殘存癌細胞存在,移植入三分之二的活體肝臟後,肝臟會再生,癌細胞也會跟著再生;其再生速度會比屍肝移植快一些。不過也有研究指出,活肝移植與屍肝移植的肝癌復發率沒有顯著的差異,所以目前仍沒有定論。
A:的確有這樣的說法,但目前仍無定論。主要原因是假如換肝病人體內已有殘存癌細胞存在,移植入三分之二的活體肝臟後,肝臟會再生,癌細胞也會跟著再生;其再生速度會比屍肝移植快一些。不過也有研究指出,活肝移植與屍肝移植的肝癌復發率沒有顯著的差異,所以目前仍沒有定論。
請別錯過本期其他精彩內容…
- 【總編輯的話】重新認識你的腸道菌
- 張洪量妻子肝硬化一度病危 換肝重生 「體內有顆台灣的肝臟了」
- 前外交部長歐鴻鍊肝癌病逝 藝人蔡頭罹患肝癌住院治療
- 腸道菌 如何影響肝臟與全身健康?
- 解開病毒抑制免疫系統之謎 根治慢性B肝露曙光!
- 「心」「肝」寶貝如何相互影響?
- 大腸的各種檢查
- 多發性肝癌,怎麼救?
- 【愛肝新樂園】保肝靠自力救濟 不是殘劑
- 口乾、口苦、口臭⋯ 消化有問題嗎?
- 我該做酒精代謝酶基因檢測嗎?
- 胰臟難檢查, 如何掌握胰臟健康?
- 肝爹信箱 有問必答
- 「今年超了沒?」 華中扶輪傳愛 為弱勢民眾守護健康
- 全台腹超大連線 12家醫院總動員
- 動脈硬化4問 林鴻儒醫師專業解答
- 青春痘5問 林明秀醫師專業解答
- 慢性病管理5問 劉珈麟醫師專業解答
- 攝護腺肥大5問 周淇業醫師專業解答
- 幽門桿菌4問 謝睿穎醫師專業解答
- 【好心肝故事】沒有B肝、也沒有C肝 施伯南先生 每年一「超」,及早發現肝癌
- 好心肝門診中心即將擴建11樓診間服務 懇請各界愛心響應襄助