
第87期
出刊日:2019-07-15
返回上一層熱門話題/細胞治療開放上路 自體免疫細胞可當抗癌解藥
衛生福利部2018年9月發布《特定醫療技術檢查檢驗醫療儀器施行或使用管理辦法》修正條文(以下簡稱特管辦法),開放6項自體細胞治療技術,陸續已有醫學中心提出治療計畫申請且獲得通過。對使用既有療法效果不彰的癌症病人來說,自體免疫細胞療法是爭取一線生機的機會,唯療效如何個體差異大,費用也需上百萬元,仍需抱持謹慎態度面對。
諮詢/何弘能(臺大醫學院名譽教授、臺北醫學大學總顧問)
撰稿/張雅雯、黃靜宜
被視為癌症治療新突破的免疫療法(尤其是免疫檢查點抑制劑)還方興未艾,近期因為《特管辦法》上路,細胞療法又成為另一波熱潮。到底什麼是細胞療法?
舉凡用自己的細胞或他人的細胞,經體外培養等程序擴增細胞數目,再打回病人體內,以達到治療目的的方式,都算是廣義的細胞治療。其治療標的不限於癌症,此次《特管辦法》開放的6項細胞治療技術,除了癌症以外,還包括缺血性腦中風、皮膚燒傷、退化性關節炎、脊髓損傷等多項。比如自體軟骨細胞移植用於膝關節軟骨缺損、自體脂肪幹細胞移植用於大面積燒傷及困難癒合傷口等。
此次開放僅限自體細胞
不過,雖然細胞治療也包括使用他人細胞的方式,但此次《特管辦法》開放的範圍僅限於「自體細胞」(包括自體免疫細胞或自體幹細胞等),因為使用異體細胞容易產生排斥作用、免疫失控、傳染疾病等,風險比較高。
而自體幹細胞又只開放成體幹細胞,不包括胚胎幹細胞,因為胚胎幹細胞分化力強、穩定度低,有很多不確定性,需要另訂規範,所以不在《特管辦法》開放之列。
自體免疫細胞治療 日本已有多年經驗
總括來說,這次開放的6大項目中,最為人關注的還是自體免疫細胞治療這一部份,因為這對於一些使用現有療法仍效果不彰的癌症病人來說,是另一線救命希望。
癌症治療一般是以手術切除為首選,若無法開刀,還有化學治療、放射線治療、標靶藥物等選項,但是癌細胞太聰明、會不斷演化,因此控制癌細胞需要更有效的武器。很久以前就有研究提出,人體自身的免疫細胞夠強的時候,可以去殺死癌細胞,且理論上用自己的細胞,副作用會比較少,更能除惡務盡來減少癌細胞的復發,因此免疫細胞一直都是治療癌症的方法之一。
其實國外做免疫細胞治療已行之有年,尤其鄰近的日本,因為臨床試驗規定較寬鬆,細胞治療已經施行多年,台灣因為法規始終沒有跟上,免疫細胞治療一直沒有發展起來,導致想尋求此一療法的病患只能跨海求醫。一直到今年,終於等到《特管辦法》上路。
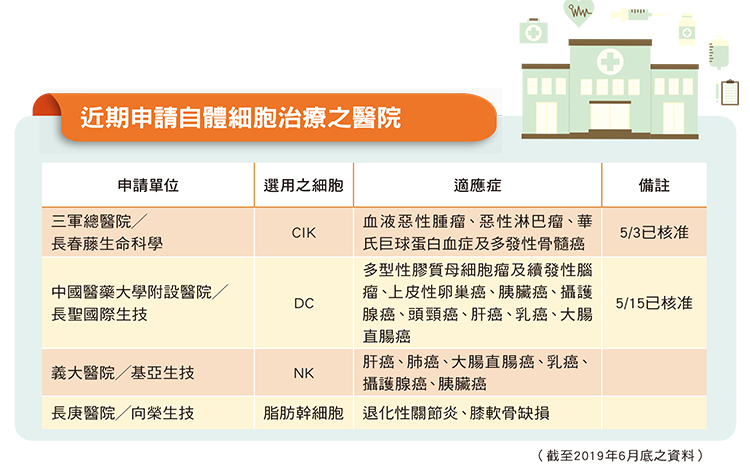
此次開放的6種自體免疫細胞治療,取決條件是比較安全、副作用較少、文獻上稍微有點證據的,包括NK、DC、CIK、DC-CIK、TIL、gamma-delta T 這幾種免疫細胞;適用對象則是經標準治療無效的血液惡性腫瘤或第一至第三期實體癌病人,以及實體癌第四期的病患。不過,目前成效比較好的還是血液腫瘤。

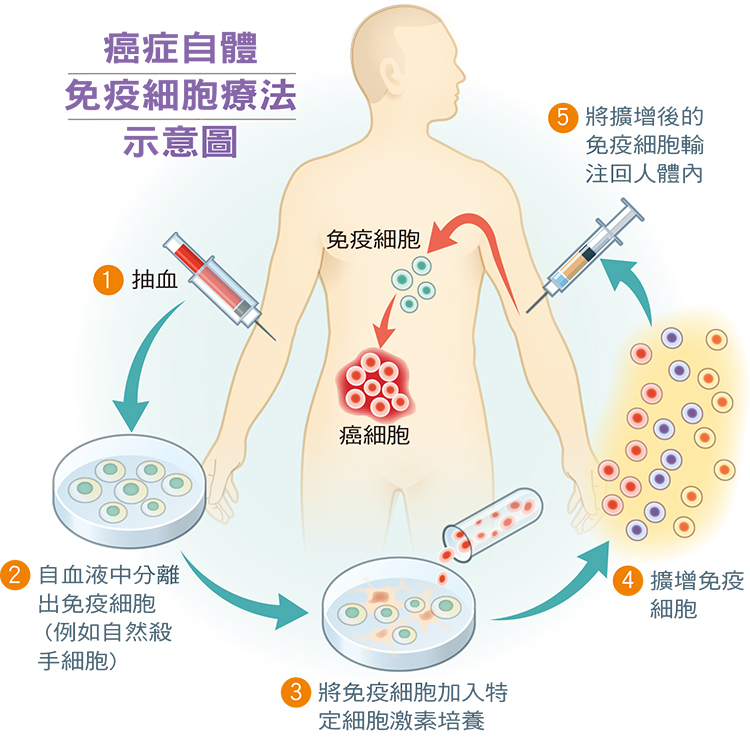
免疫細胞體外培養擴增後 輸回體內殲滅癌細胞
自體免疫細胞治療是取出病人的免疫細胞,加以培養、誘導、活化及擴增數量後,再輸回病人體內去對抗癌細胞。免疫細胞有很多種,最早有研究選用自然殺手細胞(Natural Killer Cell, NK),試驗對象是從黑色素細胞瘤(皮膚癌的一種)開始,初期成果不錯,後來發現癌細胞也沒那麼笨、會隨時調整,像NK細胞這種屬於免疫細胞的先鋒部隊,對於「敵人」的辨識能力較差,尤其癌細胞很會偽裝,當NK細胞沒有足夠的數量或特異性時,未必能殺死癌細胞。
因此後來有研究改用樹突細胞(Dendritic Cell, DC),有突刺的樹突細胞是扮演「偵查兵」的角色,可搜索、識別癌細胞,再指揮可以作戰的T細胞上戰場殺敵,雖然這樣確實增加抗癌效果,但後來也發現大概僅10~30%有效,於是又有研究嘗試「雞尾酒療法」,就是把這些免疫細胞加在一起來運用,但效果仍有限。
基因改造後的CAR-T攻擊力更強 台灣尚未開放
這時開始有人在想,是不是免疫細胞的數目不夠多?如何讓主攻的T細胞增加對付癌細胞的攻擊力?於是出現嵌合抗原受體T細胞(Chimeric Antigen Receptor T Cells, CAR-T),這是利用基因改造的技術,讓T細胞增加數量、特異性以及毒殺癌細胞的力量,並且把辨識癌細胞的受體放在T細胞身上,再將這個改造後的T細胞輸回病患體內,讓T細胞如同裝了雷達,可精準殲滅癌細胞。
CAR-T的出現在一些個案報告中效果很好,然而強力的武器也讓患者承受更大的副作用,因為這個療法有可能導致體內大量細胞激素釋放,病患可能出現呼吸困難、發高燒、低血壓等副作用,往往需要住到加護病房,而且這樣的免疫風暴若沒有妥善處理,反而會致命。
後來整體統計發現,CAR-T治療的效果也僅20~30%,且副作用很大;另一個問題是價格昂貴,換算台幣,治療一個病患要花費1千多萬元,受惠者極其有限。
而CAR-T因為將細胞做基因改造,改變了細胞原有的生物特性,流程比較複雜,而且治療過程有極高引起免疫風暴的風險,要做必須申請臨床試驗,所以不在這次開放之列。

免疫細胞治癌個別化差異大
存在許多未知數
免疫細胞治療雖然是抗癌的新顯學,但患者接受免疫細胞治療的效果,個別差異很大。因為細胞培養處理上不像單一藥物相對穩定,製程當中是否可能有感染或不好的化學物質跑進去?免疫細胞大量培養輸回體內後,會產生什麼結果?經常是因人而異,有很多不確定性。因此,對於癌症病人來說,若是癌症1~3期,建議還是先接受有較多科學證據的標準治療,如果都無效再考慮自體免疫細胞治療。
此次《特管辦法》的開放,除了給癌症病人一線希望,也希望藉此蒐集更多資料分析,之後就能比較清楚什麼樣的病人,接受此療法有較大的成功機會,達到所謂精準醫療。
對於申請執行細胞治療的單位,也要求必須符合規定,例如實驗室需認證,執行的醫療人員必須接受細胞治療、倫理、法規相關的教育學分訓練,來確保品質與安全。在費用方面也有把關,目前幾個醫學中心提出來的計劃,一個療程約在台幣200萬元上下。
免疫細胞擴增數量及品質
也是治療成功與否的關鍵
免疫細胞治療要成功,選擇哪種免疫細胞、用在哪種癌症以及病人本身的條件都是重點。另外,實驗室每一個流程、環節也會影響效果,所以免疫細胞治療很難做臨床試驗,不像藥物的臨床試驗那麼單純清楚。
尤其,自病人身上抽血取出免疫細胞後,需要經過體外培養的過程,目的是將免疫細胞擴增數量,這個讓免疫細胞「壯大軍容」的方法,就牽涉到很多技術,影響了免疫細胞的品質。例如是人工培養還是靠機器自動化培養,使用哪種特定細胞激素等,每家醫院及生技業者的做法不一樣,未來也希望有所把關。
民眾最關心療效如何?免疫細胞治療大約一個月打1次,3至6個月為1個療程,療程或抗癌效果因人而異,且可能因為不同癌症、不同期別而有不同結果。但免疫細胞治療也可望做為手術後或化療的輔助療法,降低癌症復發或轉移的機率,如同免疫檢查點抑制劑也較少單獨做為抗癌使用,而是搭配其他的治療,一起力抗癌症。
幹細胞的潛力被寄予厚望
除了免疫細胞,醫療界對幹細胞治療的期望也很深,一旦成功,對醫療更是革命性的改變。比如心臟衰竭患者一旦面臨需換心救命,由於捐心者有限,若能透過幹細胞治療來達到如同「換零件」的效果,存活率將大增。只是全球投入幹細胞研究至今,尚未出現可應用於臨床的重大成果。
日本在iPS細胞(又稱誘導性多功能幹細胞、萬能細胞)領域處於全球領先位置,這是京都大學教授山中伸彌在全球率先研發成功,他從發表論文到獲得諾貝爾獎,僅短短6年,顯示日本政府投入的企圖心,現在已有多項臨床試驗利用iPS細胞來治療視網膜病變、心臟、脊椎等病變。
至於胚胎幹細胞的研究,因為在美國牽涉到倫理議題,相關研究發展也是走走停停。早期美國政府不准做胚胎幹細胞的研究,一直到歐巴馬時期,才有臨床試驗核准用胚胎幹細胞治療脊椎受傷患者,後來又有類似的試驗用於視網膜治療,但這兩個計畫後來也因為價格太昂貴等原因,沒有順利推動下去。
成體幹細胞相對安全
因此,目前為止,不論胚胎幹細胞或萬能細胞,雖然未來看起來很光明,但研究仍在試驗階段。《特管辦法》開放使用的都是自體成體幹細胞,雖然它的分化能力不像胚胎幹細胞或萬能幹細胞那麼強,但也因此相對安全,可以避免因為控制不好反而導致癌化;另一個好處是相對便宜且容易取得,也不像使用胚胎幹細胞有倫理爭議。
取用哪種細胞各有利弊,現階段最重要的是在安全的前提下,讓台灣的細胞治療逐漸上軌道,有朝一日能成為癌症病人的救命新希望。
請別錯過本期其他精彩內容…
- 總編輯的話-走出肝苦,迎向陽光
- LiverNews/肝癌二線標靶藥納健保給付 一線用藥規定放寬
- LiverNews/B肝帶原孕婦之新生兒 7月起全面補助注射免疫球蛋白
- 封面故事/最新B、C肝治療全解析
- 肝病診療室/肝癌何時需要放射治療?
- 肝病診療室/膽汁為什麼會逆流?
- 肝病診療室/您是「隱藏版」B肝帶原者嗎?
- 愛肝新樂園/拖泥帶水的肝癌
- 生活醫館/大腸鏡檢查揪出危險息肉 該切嗎?怎麼切?該注意什麼?
- 生活醫館/20年來發生率多3倍!不菸不酒也可能罹患食道癌
- 生活醫館/上腹痛,到底哪裡出問題?
- 生活醫館/慢性腹瀉,要緊嗎?
- 肝爹信箱 有問必答
- 醫療行腳/國際扶輪3522地區總動員 新北市汐止3小時篩檢2062人!
- 【請問好心肝】肝膽腸胃科5問 蔡宛玲醫師 專業解答
- 【請問好心肝】肝膽腸胃科5問 葉佳衢醫師 專業解答
- 【請問好心肝】家庭醫學科4問 吳妮民醫師 專業解答
- 【請問好心肝】身心科4問 吳思穎醫師 專業解答
- 【請問好心肝】眼科5問 黃詩瑋醫師 專業解答
- 江幸雪女士遺愛人間-母愛化為大愛,捐助好心肝病友
- 好心肝門診中心將擴充樓層及診間-籲請各界熱烈愛心襄助